Insuline en diabetes type 1: we weten en kunnen steeds meer
In 2021 is het honderd jaar geleden dat insuline werd ontdekt. Kortom tijd voor een korte terug- en vooruitblik op insuline en diabetes type 1.
De geschiedenis van insuline en insulinetherapie begon dus slechts een eeuw geleden. Deze gebeurtenis heeft de kwaliteit van leven voor mensen met diabetes ingrijpend veranderd. De ontwikkeling van insulinetherapie heeft ervoor gezorgd dat zij vrijwel een normaal leven kunnen leiden. Om de zware mentale belasting van mensen met diabetes type 1 (voornamelijk) verder te verlichten maken de nieuwste innovaties zelfs een geautomatiseerde en gepersonaliseerde insulinetoediening mogelijk. Hierdoor hoeven mensen met diabetes nog minder tijd besteden aan het beheer van hun chronische ziekte en hebben ze meer tijd voor andere, leuke dingen!
Fysiologie van insuline
Bij mensen die geen diabetes hebben wordt insuline afgescheiden door de bètacellen van de alvleesklier. Alle hormoonproducerende cellen (of endocriene cellen) zitten in de eilandjes van Langerhans die 2% van de massa van de alvleesklier vormen. De β (bèta) cellen van de eilandjes maken insuline aan. In eerste instantie gebeurt dit in de vorm van pro-insuline. Afhankelijk van de behoefte van het lichaam wordt pro-insuline omgezet naar twee stoffen:
- C-peptide, of
- Insuline.
Naast de β cellen bevatten de eilandjes de volgende cellen:
- ⍺ (alpha) cellen voor de aanmaak van glucagon,
- δ (oméga) cellen voor de productie van somatostatine, en
- PP-cellen voor de aanmaak van pancreatische polypeptide.
Bij mensen zonder diabetes gaat de inname van voedsel (en met name van koolhydraten) tijdens de maaltijd gepaard met een verhoging van de glucoseconcentratie in het bloed (glycemie). Hierdoor komt de secretie (afscheiding of afgifte) van insuline in de β-cellen van de eilandjes van Langerhans zeer snel op gang.
Eenmaal afgescheiden, zorgt insuline voor de opname van glucose uit het bloed in de cellen om energie te produceren. Dit leidt vervolgens tot een verlaging van de bloedsuikerspiegel.
In de lever bevordert insuline de opslag van de glucose in de vorm van glycogeen, in de spieren bevordert het de productie van eiwitten en in het vetweefsel speelt het een belangrijke rol bij de opslag van vetten.
Bij mensen met diabetes
Voor mensen met diabetes is de regulering van de afscheiding van insuline verstoord. Insuline wordt bij diabetes type 1 door het lichaam helemaal niet meer ‘geproduceerd’. Bij diabetes type 2 is de eerste fase van de insuline-afscheiding zodanig veranderd, dat de vrijgekomen insuline niet voldoende is om de glycemie terug te brengen naar de gewenste waarden en deze hoog blijven, vooral na een maaltijd.
Bij geen of onvoldoende insuline kan het lichaam niet meer zijn normale ‘brandstof’ (glucose) gebruiken waardoor deze niet meer in de cellen kan worden opgenomen. Het lichaam moet dan zijn reserve ‘brandstof’ gebruiken: vetten en eiwitten. Daarvoor mobiliseert het vetweefsel zijn reserves (triglyceriden, vetzuren en glycerol) en breken de spieren hun eiwitten (aminozuren) af. De lever breekt zijn glycogeenreserves snel af tot glucose en neemt aminozuren en glycerol op en zet deze om in glucose. De lever neemt ook vetzuren op en zet die om in ketonen, die worden vrijgegeven in het bloed. De spieren nemen geen glucose meer op en er ontstaat een stijging van de bloedsuikerspiegel (hyperglycemie). Als het tekort aan insuline aanzienlijk en langdurig is, ziet men niet alleen een stijging van het bloedsuiker maar ook de aanwezigheid van ketonen in het bloed en van glucose en ketonen in de urine.
WIST JE DAT?> Insuline het enige hormoon in het lichaam is met een hypoglycemische werking (dat het glucosegehalte in het bloed verlaagt)1. > Insuline gemiddeld de op zes na duurste vloeistof ter wereld is. Het komt nog voor kwik en menselijk bloed want het kost meer dan 2.000 euro per liter2. |
> Andere hormonen, de hyperglycemische, zijn betrokken bij het handhaven van de bloedsuikerspiegel, waaronder glucagon, dat wordt afgescheiden door de ⍺ cellen van de eilandjes wanneer de bloedsuikerspiegel daalt. Door de werking van deze hormonen na te bootsen al naar gelang het glycemisch peil, kan de bloedsuikerspiegel binnen het bereik van normale waarden worden gehouden.
> Insuline wordt in grote hoeveelheden aangemaakt tijdens de maaltijd en is ook nodig voor het basismetabolisme van het lichaam (de basiswerking buiten de maaltijden om).
Geschiedenis van insuline en insulinetherapie
De beginfase van synthetische insuline: een dierlijke oorsprong
De geschiedenis van ‘syntetische’ insuline voor mensen met diabetes type 1 begint bij de extractie ervan uit de alvleesklier van varkens en koeien. Deze insuline moest nog wel worden gezuiverd voordat het door mensen kon worden gebruikt. Men sprak toen van ‘normale’ insuline die in 3 of 4 injecties per dag werd toegediend met behulp van een glazen, te steriliseren injectiespuit en behoorlijk dikke naalden. De insuline moest in de koelkast worden bewaard.
In de jaren 1930-50 werden verschillende procedures ontwikkeld waarmee vormen van insuline met verlengde werking kon worden verkregen. De insuline werd echter nog steeds met injectiespuiten toegediend. Deze insuline was niet perfect gezuiverd. Onzuiverheden veroorzaakten allergieën of lokale reacties op de plek van de injectie. Men constateerde ook vaker lipodistrofieën en de productie van antilichamen tegen insuline waardoor de insuline minder effectief was.
In de jaren zeventig leidde de verwijdering van deze onzuiverheden tot chromatografisch “gezuiverde” dierlijke insuline, die monocomponent werd genoemd. Er werd toen gesproken over ‘zeer gezuiverde insuline’.
Reproductie van menselijke insuline dankzij een chemisch proces
Een belangrijke mijlpaal in de geschiedenis van insuline was de beschrijving van de chemische structuur van menselijke insuline door de biochemicus F. Sanger in 1955.
In de jaren 1980 werd dierlijke insuline vervangen door een vorm van menselijke insuline. Het werd verkregen door varkensinsuline via een chemisch proces (hemisynthese) om te zetten. Later gebeurde dit door middel van genetische manipulatie (biosynthese) van bacteriën of gist. Het belang hiervan was enorm. Deze innovatie betekende dat men nu synthetische insuline kon produceren. Hierdoor was men niet meer afhankelijk van een dierlijke bron, werd het risico op de vorming van antilichamen verminderd en kon men vanaf toen beschikken over onbeperkte hoeveelheden insuline.
De insuline-analogen
De verandering van de samenstelling van de synthetische insuline in de jaren 1990 veranderde de werkingssnelheid en -duur. Men sprak over gemodificeerde insuline of ‘insuline-analoog’, die door biosynthese werd geproduceerd. Er werd onderscheid gemaakt tussen ‘snelle analogen’: met een snelle maar kortdurende werking vergeleken met menselijke insuline; en de ‘analogen met langere werking’: middellangwerkende of langwerkende insuline.
In 1993 werden de resultaten van de Diabetes Control and Complications Trial (DCCT) gepubliceerd: het verminderen van chronische hyperglycemie, gemeten aan het HbA1c-niveau, hielp complicaties op lange termijn van diabetes type 1 te voorkomen (netvlies, nieren, zenuwen). Deze resultaten pleitten dus voor de noodzaak van een goede glycemische beheersing.
Dit was het begin van “geïntensiveerde multi-injectie” insulinebehandeling. Het concept van therapeutische voorlichting, die erop gericht was mensen met diabetes de instrumenten aan te reiken om hun chronische ziekte te beheersen, werd steeds belangrijker bij het beheer (glucosemeting, enz.). Dit was weer een belangrijke ontwikkeling in de geschiedenis van insulinetherapie.
Tegenwoordig wordt alle insuline geproduceerd door middel van genetische manipulatie. Deze synthetische insuline heeft precies dezelfde samenstelling als menselijke insuline of, in het geval van ‘insuline-analogen’, een gewijzigde samenstelling om de werkingsduur te verkorten of te verlengen. Naar gelang de werkingsduur en de snelheid waarmee de werking begint, onderscheiden we drie typen insuline: langwerkende (meer dan 24 uur), middellangwerkende (12 uur) en snel werkende (2 tot 4 uur).
Geschiedenis van de insulinetherapie: Innovatieve oplossingen
Apparaten voor de beheersing van diabetes: Insulinepompen, insulinepennen en bloedglucosemeters
In de jaren ’80 van de vorige eeuw werd de insulinepomp geïntroduceerd. De pomp geeft permanent insuline af aan het lichaam en bootst zo de functies van de alvleesklier na van iemand die geen diabetes heeft.
In diezelfde periode zorgden de eerste pennen met insuline-ampullen ervoor dat er minder injectiespuiten en flesjes gebruikt hoefden te worden. Ze werden opgevolgd door vooraf gevulde wegwerpspuiten ook wel ‘insulinepennen’ genoemd, een nog eenvoudigere manier om zelf insuline in te spuiten. Dit was een revolutie in de insulinetherapie. Het betekende het einde van de glazen injectiespuiten en het hergebruik van naalden die in kokend water gesteriliseerd moesten worden.
Hiernaast werden de eerste capillaire bloedglucosemeters steeds kleiner en verfijnder. Zij hadden nog slechts enkele druppeltjes bloed nodig om goed te werken. De betrouwbaarheid van de meters werd ook steeds groter.
Doorlopend glucose meten
Het zelf beheersen van bloedglucose was ook een grote stap voorwaarts in de geschiedenis van de insulinetherapie met de verschijning van de eerste apparaten voor doorlopende glucosemeting (CGM). Hiermee kon de interstitiële glucosespiegels vrijwel onmiddellijk en gedurende meerdere dagen worden gecontroleerd en zo dicht mogelijk bij de capillaire bloedglucosewaarden worden gehouden.
Middelen en technieken: hoe staat het daar nu mee?
Insuline bij diabetes type 1 wordt nu vooral zelf en onderhuids toegediend. Mensen met diabetes gebruiken, afhankelijk van de werking: een langwerkende, langzaam- of middellangwerkende insuline om in hun basale insulinebehoeften te voorzien en een kort- en snelwerkende insuline voor de maaltijden. De combinatie van langzame en snelle insuline is ontworpen om de fysiologie van insuline in het lichaam zo goed mogelijk na te bootsen en is bedoeld om de suikerspiegel dicht bij normale waarden te houden.
Snelle insuline-‘analogen’ verkorten de tijd tussen de injectie en de maaltijd wat vooral praktisch is als mensen uit eten gaan (restaurants, kantines, fastfoodrestaurants). Dit heeft geleid tot de ontwikkeling van ‘functionele insulinetherapie’ of ‘koolhydratentelling’, gebaseerd op een schatting van de dosis insuline bij de maaltijd, al naar gelang van de ingenomen hoeveelheid koolhydraten. Een kortere werkingsduur vermindert het risico van hypoglycemie lang na de maaltijd, of in het geval van cumulatieve doses, tussen twee maaltijden in.
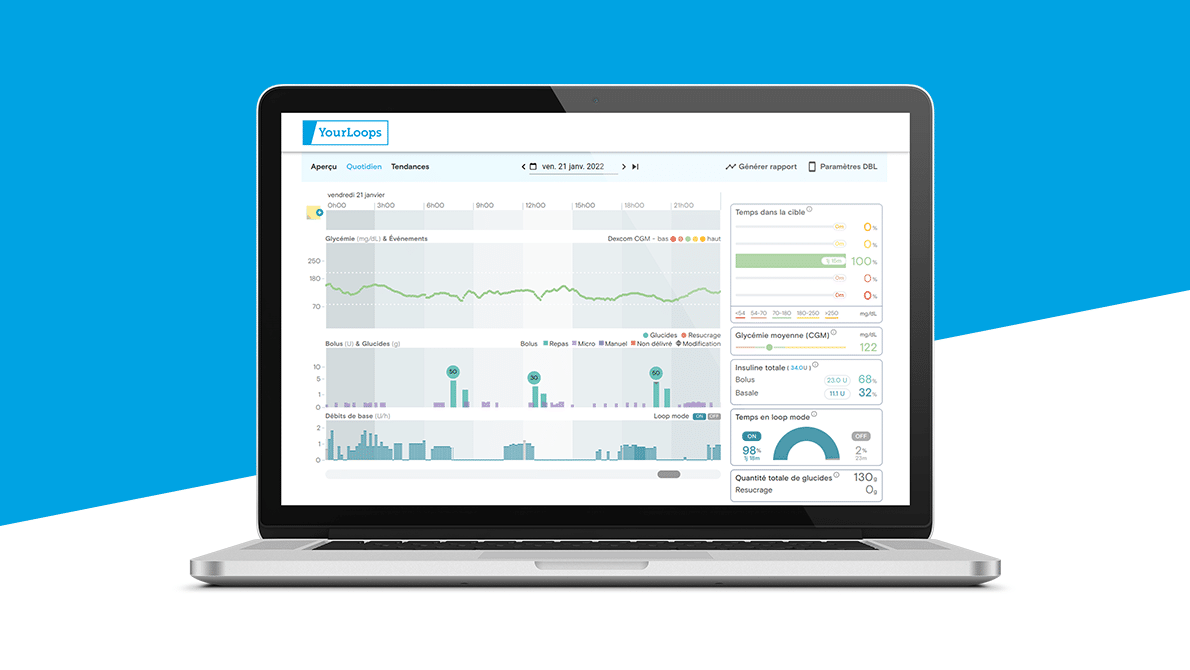
Subcutane insulinepompen, waarmee uitsluitend snelle insuline wordt toegediend, maakt gebruikt van de snellere en kortere insuline. Dit wordt vooral gebruikt in geautomatiseerde systemen voor insulinetoediening (ook ‘gesloten lus’ of ‘semi-gesloten lus’ systemen genoemd) die een beslissingsondersteunend algoritme, een sensor voor doorlopende glucosemeting (CGM) met een insulinepomp in-één combineren. De insulinetoediening wordt automatisch bijgesteld aan de hand van de bloedglucosewaarden die door de continu glucosemeter wordt doorgegeven.
Nog een recente ontwikkeling tenslotte, is dat in bepaalde specifieke gevallen in gespecialiseerde centra ook de toediening van insuline door transplantatie van eilandjes van Langerhans wordt overwogen.3, 4, 5, 6
Een terugblik op de geschiedenis van insuline laat zien dat er belangrijke voortuitgang is geboekt. De vooruitblik voor het controleren van insuline bij diabetes (type 1) ziet er dan ook goed uit!
BIBLIOGRAFIE
- J. Girard. Les actions physiologiques de l’insuline. MÉDECINE DES MALADIES MÉTABOLIQUES. Vol 2 – N° S2. P. 124-129 – 12/2008
- https://beyondtype1.org/the-10-most-expensive-liquids-in-the-world/#:~:text=Insulin%20%249%2C400*%20per%20gallon,produce%20in%20its%20biosynthetic%20form.
- G. Slama. Histoire de l’insulinothérapie. MÉDECINE DES MALADIES MÉTABOLIQUES. Vol 6 – N° 4. P. 352-357 – 09/2012
- Nathan DM. Long-term complications of diabetes mellitus. N Engl J Med 1993;328:1676-85.
- B.Vialettes, D.Raccah. Les analogues de l’insuline. JOHN LIBBEY EUROTEXT. 2006
- S. Halimi, N. Wion, A.-L. Coulon, P.-Y. Benhamou. Les insulines, ultra-rapides, et techniques pour accélérer l’action des insulines rapides. MÉDECINE DES MALADIES MÉTABOLIQUES. Volume 8, Issue 2, Pages 125-132. 07/2014.